为什么总是吃不饱?华人学者张召最新Science揭示大脑纤毛发挥了关键作用
2025-09-15 08:00来自翻译狗阅读1
在节食与意志力之间苦苦挣扎的人们,或许并未意识到,控制食欲的关键,可能藏在大脑神经元上的一根细小纤毛里。
2025年6月5日,德克萨斯大学西南医学中心张召团队在Science杂志发表研究,发现一种名为GPR45的G蛋白偶联受体,在调控进食行为中发挥关键作用。研究显示,GPR45 并不直接传递信号,而是负责把一个关键的信号分子“送”到正确的位置——大脑神经元的初级纤毛(primary cilia)。
这个定位过程一旦失效,饱腹信号链条随之中断,大脑便误以为身体仍处于饥饿状态,从而触发持续进食,最终导致肥胖。该论文题为:GPR45 modulates Gαs at primary cilia of the paraventricular hypothalamus to control food intake,由寻禹与蒋怡翱为共同第一作者。

研究起始于一项基于随机诱变的大规模小鼠正向遗传学筛选。在两个独立的突变谱系中,研究人员观察到极端的肥胖表型。通过自动化连锁分析(automatic meiotic mapping),两个致病点突变均被定位至Gpr45基因。Gpr45基因敲除小鼠重现了同样的肥胖表型,然而,GPR45缺失并未显著改变小鼠的能量消耗或活动水平,但进食量明显增加。配对喂养(pair-feeding)实验显示,通过控制食物摄入量,这些突变小鼠的体重可以恢复正常,表明食欲失调是导致肥胖的直接原因。
进一步研究发现,GPR45蛋白在下丘脑室旁核(PVH)中高度表达。该区域是调控摄食的关键神经中枢,富含MC4R等经典信号通路的核心因子。值得注意的是,GPR45 并不均匀分布在神经元表面,而是精准定位于初级纤毛之上。初级纤毛被认为是神经元的信号接收平台,多个调控摄食的关键通路(如MC4R-ADCY3)都在这里定位,但调控其功能的分子机制并不清楚。
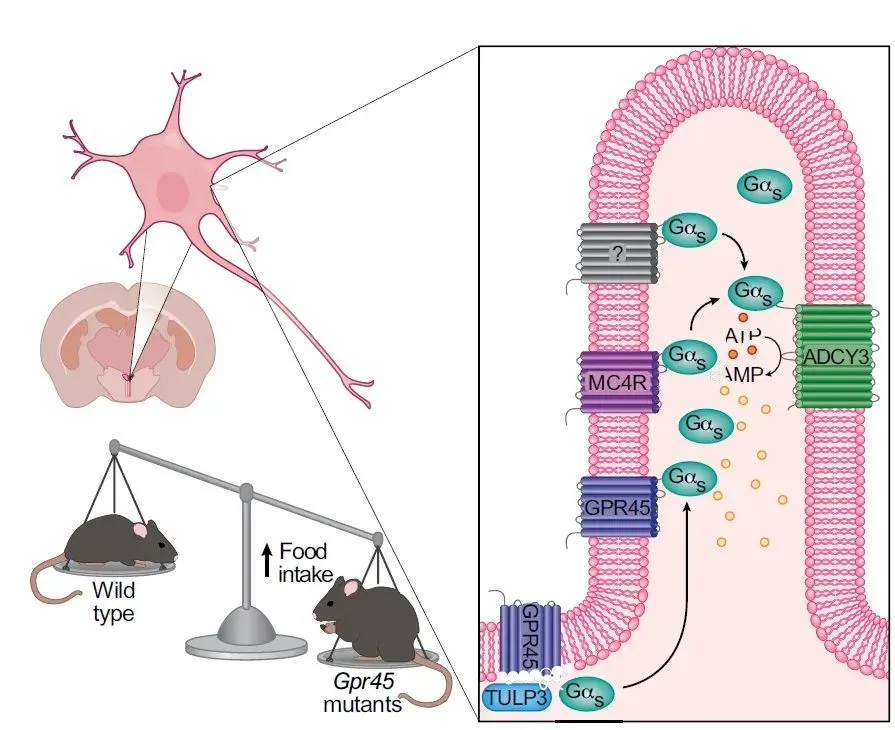
机制层面显示,GPR45 并不直接激活任何下游信号分子,而是作为转运因子,将 Gαs蛋白引导进入纤毛。Gαs是一个重要的信号传递分子,位于MC4R的下游,能够激活腺苷酸环化酶 ADCY3,产生cAMP 并抑制进食。GPR45 缺失后,Gαs无法进入纤毛,ADCY3 不能被激活,饱腹信号链路中断,导致大脑“误判”身体处于饥饿状态,进而驱动持续进食。
而之前发现的两个GPR45点突变(S214P 和 Y287C),虽然并未影响蛋白本身的表达,但均破坏了其进入纤毛和转运Gαs的能力。这类突变也同样无法恢复小鼠的正常摄食行为,进一步证明 GPR45 的“定位功能”而非信号转导本身,是其调控食欲的关键。
尽管本研究尚未直接检测 GPR45 在人类组织中的表达或功能,但从序列高度保守性和下丘脑区域的功能对比推测,这一机制在人类中可能同样存在。考虑到 GPCR 是当前药物开发中最成熟的靶点家族,而最近广受关注的 GLP-1 类减肥药也属于该类受体,GPR45 作为一种以“空间定位”而非激活信号为核心功能的受体,为开发新型抗肥胖疗法提供了新思路。
这项工作带来的启发不仅仅是一条新的信号通路,更是一种理解中枢调控的方式转变。大脑对能量状态的判断,依赖一整套复杂而精密的分子组织系统,而这些系统的正常运作,或许只需要某一个分子“准确地出现在它该在的位置上”。而当这种“空间错位”发生,即便通路本身并未被破坏,也足以引发系统性失调。
也因此,这根被长期忽视的纤毛,开始在代谢研究中扮演越来越核心的角色。它既是神经元的信息中转站,也可能是饥饿与饱腹、节制与冲动之间的关键转折点。未来针对中枢性肥胖的治疗,也许不只是刺激或阻断某一通路,而是重新建立那些在微观尺度上“错位”的连接。
从神经元的纤毛出发,这项研究连接了分子定位、信号传导与行为调控三大层次,为理解肥胖的中枢机制打开了一条新的通道。在科学探索“吃不饱”的问题背后,我们看到的其实是大脑内部一次精准而脆弱的信息传递,而一根纤毛,或许正是这套系统能否正常运行的关键。
原文链接https://doi.org/10.1126/science.adp3989





